I. Prezentare generală aESMOGhidul din 2025
În august 2025, ESMO a lansat oficial Ghidul de practică clinică ESMO pentru diagnostic, tratament și urmărire, intitulat „Cancerul pulmonar fără celule mici, în stadiu incipient și local avansat: Ghidul ESMO pentru diagnostic, tratament și urmărire”, publicat în revista de oncologie de renume, Annals of Oncology. Aceasta este prima actualizare cuprinzătoare de la versiunea din 2017 și oferă o referință extrem de autorizată pentru oncologii din întreaga lume.

Cancerul pulmonar are cea mai mare incidență și mortalitate dintre toate tumorile maligne la nivel global. În fiecare an, există peste 2,2 milioane de cazuri noi și peste 1,8 milioane de decese, ceea ce face ca acest cancer să fie principala cauză de deces legat de cancer, atât la bărbați, cât și la femei. Cancerul pulmonar fără celule mici (NSCLC) reprezintă aproximativ 80-85% din totalul pacienților cu cancer pulmonar. În acest context grav, publicarea ghidului din 2025 injectează un nou impuls științific în practica clinică, actualizarea strategiilor de testare a biomarkerilor fiind deosebit de importantă.
II. Interpretarea actualizărilor cheie ale ghidului
2.1 Testarea biomarkerilor: de la „opțională” la „esențială”
Ghidul din 2025 aduce o modificare strategică importantă în ceea ce privește testarea biomarkerilor. Ghidul precizează în mod explicit că testarea biomarkerilor este esențială pentru luarea deciziilor de tratament la pacienții cu NSCLC în stadiul IB-III.
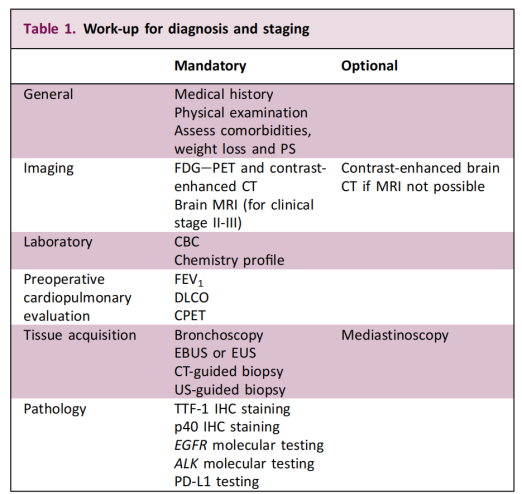
Această recomandare extinde testarea moleculară de la concentrarea anterioară asupra pacienților cu boală avansată la cazurile rezecabile în stadiu incipient. Obiectivul principal este de a identifica mutațiile genetice driver și de a oferi o bază științifică pentru un tratament personalizat de precizie. Ghidul subliniază, de asemenea, că fezabilitatea biopsiei și a abordării diagnostice ar trebui determinate de o echipă multidisciplinară pe baza caracteristicilor pacientului și ale tumorii.
În ceea ce privește strategia specifică de testare, ghidul recomandă în mod clar ca testarea genetică să fie efectuată înainte de luarea deciziei chirurgicale și ca aceasta să acopere cel puțin EGFR și ALK. Acest concept de „testare în avans” are o semnificație clinică profundă pentru stratificarea precisă și tratamentul personalizat al NSCLC în stadiu incipient – promptitudinea și acuratețea rezultatelor testelor determină direct alegerea terapiei adjuvante ulterioare.
2.2 Descoperiri terapeutice în NSCLC în stadiu incipient, pozitiv pentru oncogenele driver
Ghidul din 2025 integrează dovezi din mai multe studii clinice majore pentru a stabili o cale de tratament clară și precisă pentru pacienții cu NSCLC în stadiu incipient, pozitiv pentru oncogena driverului.
Pacienți cu mutație EGFR pozitivă:Pe baza studiului clinic ADAURA, tratamentul adjuvant postoperator cu osimertinib timp de trei ani a devenit standardul global de îngrijire pentru pacienții cu deleții ale exonului 19 al EGFR sau mutații ale exonului 21 L858R. Studiul ADAURA este un studiu internațional, multicentric, randomizat, controlat, de fază III, care evaluează eficacitatea și siguranța osimertinibului adjuvant la pacienții cu NSCLC cu mutație EGFR în stadiul IB-IIIA, complet rezecat. Studiul a arătat că osimertinibul a îmbunătățit semnificativ atât supraviețuirea fără boală, cât și supraviețuirea generală în comparație cu placebo, stabilind osimertinibul ca noul standard de îngrijire pentru această populație. Cu toate acestea, analizele exploratorii ale studiului ADAURA au indicat că aproximativ 36% din întreruperile timpurii ale tratamentului au fost determinate de evenimente adverse, iar alte 31% s-au datorat deciziei pacientului. Această constatare subliniază necesitatea unor teste inițiale precise înainte de tratament, pentru a se asigura că terapia țintită este administrată pacienților care pot obține beneficii susținute.
Pacienți ALK-pozitivi:Pe baza studiului ALINA, alectinib adjuvant postoperator timp de doi ani este acum standardul de îngrijire. În analiza primară a studiului ALINA randomizat, deschis, de fază III, alectinib-ul a demonstrat un beneficiu semnificativ în ceea ce privește supraviețuirea fără boală la populația în stadiul II-IIIA, cu un raport de risc de 0,24. Datele actualizate din studiul ALINA, prezentate la congresul ESMO 2025, au arătat că, după ≥3 ani de urmărire, beneficiul DFS al alectinib-ului a rămas „menținut și semnificativ clinic”, cu un raport de risc de 0,36 la populația în stadiul II-IIIA. Cea mai recentă rată globală de supraviețuire la 4 ani raportată a atins 98,4%, rata DFS la 4 ani a fost de 75,5%, iar DFS la nivelul sistemului nervos central s-a îmbunătățit și ea, fără noi semnale de siguranță. Aceste date robuste stabilesc în continuare alectinib-ul adjuvant ca standard de îngrijire după rezecția NSCLC ALK-pozitiv și subliniază valoarea testării precise pentru identificarea acestor pacienți.
Alegerea metodei de testare:Ghidul ESMO din 2025 enumeră în mod explicitteste multiplex RT-PCR pe panourialături de NGS, IHC și FISH bazate pe ARN, ca una dintre abordările tehnice recomandate pentru detectarea fuziunii ALK. Aceasta indică faptul că cerința principală a ghidului este de a efectua teste pentru a ghida deciziile clinice, mai degrabă decât de a impune o platformă de testare specifică. Pentru produsele RT-PCR axate pe detectarea EGFR și ALK, această strategie de testare flexibilă oferă o justificare solidă, bazată pe ghiduri, pentru utilizarea lor în practica clinică.
III. Soluții tehnice de testare a preciziei
Ghidul din 2025 avansează testarea către etapa de luare a deciziilor preoperatorii, ceea ce ridică ștacheta pentru acuratețea, sensibilitatea și accesibilitatea testelor. Cele două produse de detecție bazate pe RT-PCR descrise mai jos se aliniază exact cerințelor ghidului din punct de vedere tehnic.
Kit de detectare a mutațiilor EGFR 3.1 – Platformă tehnologică ARMS îmbunătățită
Tehnologie de bazăTehnologia ARMS îmbunătățită permite amplificarea specifică a secvențelor mutante cu abundență redusă pe un fond de tip sălbatic ridicat
Trei garanții tehnice:
-ARMS îmbunătățit → îmbunătățește recunoașterea mutațiilor
Îmbogățire enzimatică → digeră fondul de tip sălbatic și îmbogățește secvențele mutante
-Blocarea temperaturii → suprimă amplificarea nespecifică
PerformanţăSensibilitateaFrecvența alelelor mutante 1%
Controlul contaminăriiControl intern încorporat + enzima UNG previne contaminarea
Timp de procesareFuncționare cu tub închis, aproximativ120 de minute
Compatibilitatea eșantionului:Țesut/biopsie lichidămostre → abordează cerința de „testare în avans”
Acoperire:45 de mutațiiîn exonii 18-21 ai EGFR, care corespund exact regiunilor evidențiate conform ghidurilor (deleții ale exonului 19 și exonul 21 L858R)
Utilizare clinicăGhidează direct terapia cu EGFR-TKI
Kit de detectare a fuziunii 3.2 MMT EML4-ALK – Soluție de detectare a fuziunii pe bază de ARN

-Platformă tehnologicăRT-PCR bazată pe ARN – oferă avantaje inerente față de metodele bazate pe ADN pentru detectarea fuziunii
-Avantajul bazat pe ARNDetectează direct transcrierile de fuziune exprimate, evitând eficient rezultatele fals negative
-Dovezi ale studiuluiÎn fuziunile ALK cu abundență scăzută, RT-PCR este semnificativ mai fiabilă decât testele bazate pe ADN
-SensibilitateDetectează fuziuni până la20 de copii per reacție
-Acoperirea variantelorHuse12 variante comune de fuziune EML4-ALK(inclusiv varianta 1 ~33%; variantele 3a/3b împreună ~29%)
-Operare și control al contaminăriiTub închis, ~120 minute; controale de proces încorporate + enzima UNG previn rezultatele false
-Compatibilitatea instrumentelorCompatibil cu diverse instrumente PCR în timp real obișnuite
-Alinierea ghidurilorÎn mare măsură, în conformitate cu ghidul ESMO
IV. Coerența dintre teste și recomandările din ghid
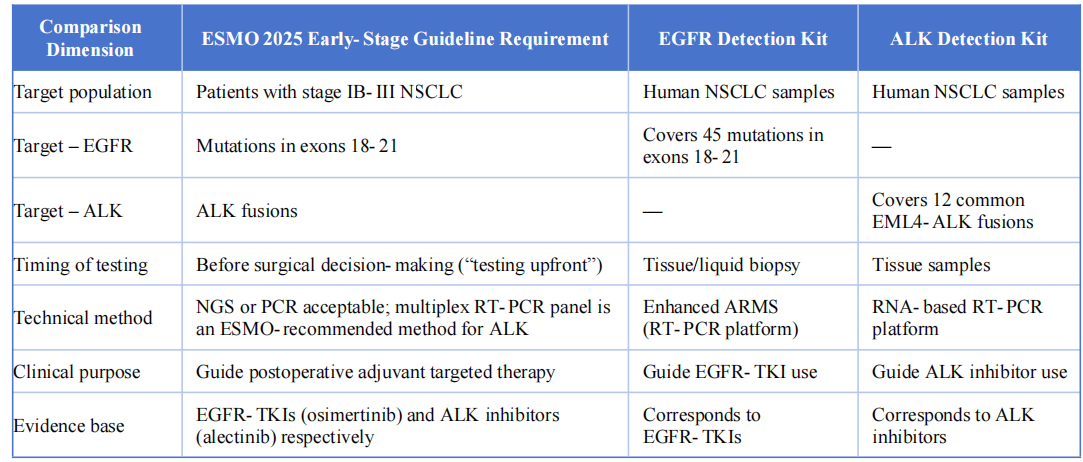
Cele două produse de detectare sunt în concordanță cu ghidul ESMO 2025 privind cancerul pulmonar fără celule mici, în stadiu incipient și local avansat, în următoarele aspecte cheie:
V. Concluzie
Ghidul ESMO 2025 pentru NSCLC în stadiu incipient deschide o nouă eră a diagnosticului și tratamentului de precizie, centrată pe „testare în avans, direcționare precisă și optimizarea tratamentului.„Kitul de detectare a mutațiilor EGFR și kitul de detectare a fuziunii MMT EML4-ALK îndeplinesc cerințele ghidului privind ținte, sincronizare și precizie prin căi tehnice distincte.”
Kitul EGFR utilizează tehnologia ARMS îmbunătățită pentru detectarea de înaltă sensibilitate a mutațiilor țintite în probe limitate, suportând atât biopsia tisulară, cât și cea lichidă pentru a permite „testarea în avans”.
Kitul ALK se bazează pe RT-PCR bazat pe ARN, oferind avantaje față de metodele ADN pentru detectarea fuziunii, aliniindu-se cu recomandarea ESMO privind panelurile RT-PCR multiplex pentru testarea ALK.
Împreună, aceste două produse formează o soluție de testare de precizie, conformă cu ghidul ESMO 2025, care susține terapia adjuvantă personalizată pentru NSCLC în stadiu incipient.
Referințe:
- Zer A, Ahn MJ, Barlesi F și colab. Cancer pulmonar fără celule mici, în stadiu incipient și local avansat: Ghidul ESMO de practică clinică pentru diagnostic, tratament și monitorizare. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Data publicării: 06 mai 2026

