Rezistența la acidul nucleic și rifampicină la Mycobacterium Tuberculosis
Numele produsului
HWTS-RT074B-Kit de detectare a acidului nucleic și a rezistenței la rifampicină Mycobacterium Tuberculosis (curbă de topire)
Certificat
CE
Epidemiologie
Mycobacterium tuberculosis, pe scurt bacilul tuberculos, TB, este bacteria patogenă care provoacă tuberculoza. În prezent, medicamentele antituberculoase de primă linie utilizate în mod obișnuit includ izoniazida, rifampicina și hexambutolul etc. Medicamentele antituberculoase de a doua linie includ fluorochinolonele, amikacina și kanamicina etc. Noile medicamente dezvoltate sunt linezolid, bedaquilina și delamani etc. Cu toate acestea, din cauza utilizării incorecte a medicamentelor antituberculoase și a caracteristicilor structurii peretelui celular al Mycobacterium tuberculosis, Mycobacterium tuberculosis dezvoltă rezistență la medicamentele antituberculoase, ceea ce aduce provocări serioase pentru prevenirea și tratamentul tuberculozei.
Rifampicina a fost utilizată pe scară largă în tratamentul pacienților cu tuberculoză pulmonară încă de la sfârșitul anilor 1970 și are un efect semnificativ. A fost prima opțiune pentru scurtarea chimioterapiei pacienților cu tuberculoză pulmonară. Rezistența la rifampicină este cauzată în principal de mutația genei rpoB. Deși apar constant noi medicamente antituberculoase, iar eficacitatea clinică a pacienților cu tuberculoză pulmonară a continuat să se îmbunătățească, există încă o lipsă relativă de medicamente antituberculoase, iar fenomenul utilizării iraționale a medicamentelor în clinică este relativ ridicat. Evident, Mycobacterium tuberculosis la pacienții cu tuberculoză pulmonară nu poate fi complet eliminată în timp util, ceea ce duce în cele din urmă la diferite grade de rezistență la medicamente în organismul pacientului, prelungește cursul bolii și crește riscul de deces al pacientului.
Canal
| Canal | Canale și fluorofori | Tampon de reacție A | Tampon de reacție B | Tampon de reacție C |
| Canal FAM | Reporter: FAM, Quencher: Niciunul | rpoB 507-514 | rpoB 513-520 | 38KD și IS6110 |
| Canalul CY5 | Reporter: CY5, Quencher: Niciunul | rpoB 520-527 | rpoB 527-533 | / |
| Canal HEX (VIC) | Reporter: HEX (VIC), Quencher: Niciunul | Control intern | Control intern | Control intern |
Parametri tehnici
| Depozitare | ≤-18℃ În întuneric |
| Termen de valabilitate | 12 luni |
| Tipul de specimen | Spută |
| CV | ≤5,0% |
| Nivel de detaliere (LoD) | Mycobacterium tuberculosis 50 bacterii/ml tip sălbatic rezistent la rifampicină: 2x103bacterii/mL mutant homozigot: 2x103bacterii/mL |
| Specificitate | Detectează Mycobacterium tuberculosis de tip sălbatic și situsurile de mutație ale altor gene de rezistență la medicamente, cum ar fi katG 315G>C\A, InhA-15C>T, rezultatele testelor nu arată rezistență la rifampicină, ceea ce înseamnă că nu există reactivitate încrucișată. |
| Instrumente aplicabile: | Sisteme PCR în timp real SLAN-96P Sistem PCR în timp real BioRad CFX96 Sistem PCR în timp real LightCycler480® |
Flux de lucru
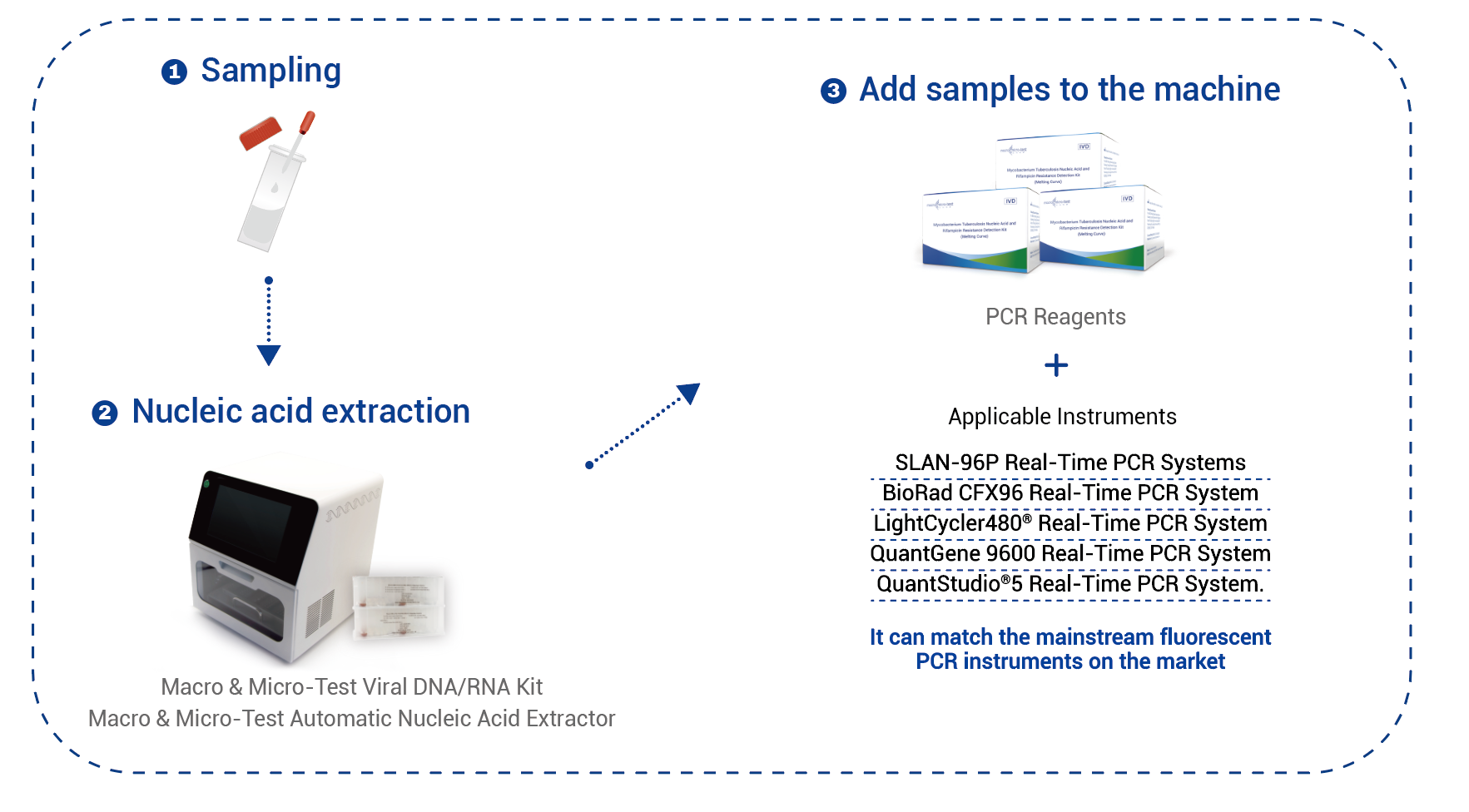
Dacă se utilizează kitul Macro & Micro-Test General DNA/RNA (HWTS-3019-50, HWTS-3019-32, HWTS-3019-48, HWTS-3019-96) (care poate fi utilizat cu extractorul automat de acid nucleic Macro & Micro-Test (HWTS-3006C, HWTS-3006B)) sau coloana Macro & Micro-Test Viral DNA/RNA (HWTS-3022-50) de la Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. pentru extracție, adăugați secvențial 200 μL de control pozitiv, control negativ și probă de spută procesată care urmează a fi testată și adăugați separat 10 μL de control intern în proba de control pozitiv, control negativ și probă de spută procesată care urmează a fi testată, iar pașii următori trebuie efectuați cu strictețe conform instrucțiunilor de extracție. Volumul probei extrase este de 200 μL, iar volumul de eluție recomandat este de 100 μL.